四.计算题(10分)(保留1位小数)

47.右图是“△△牌”钾肥的部分信息:
根据该信息计算:
(1)硫酸钾中各元素的质量比;
(2)该钾肥中钾元素的含量最高为多少?
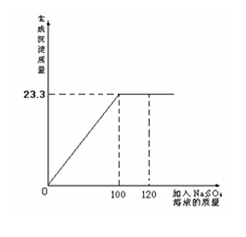
(1)生成沉淀的质量是多少?
(2)所得溶液中溶质的质量分数为多少?
化学参考答案及评分意见
一.(每小题2.5分,共35分)
题号17181920212223
答案BBDCBAD
题号24252627282930
答案CCDBDDA
二.(每空1分,共14分)
41.(2分)(1)NaCl (2)④ 。
42.(3分)(1)用锅盖盖灭;(2)6HCl+2Al(OH)3=2AlCl3+6H2O;(3)增大;
43.(4分)(1)8;(2)17;(3)Ca2+,(4)(NH4)2SO4等。
44.(5分)(1)H2O,NH3;(2)Fe2O3+3CO=2Fe+3CO2;(3)Fe2O3+6HCl=2FeCl3+3H2O;2FeCl3+Fe=3FeCl2。
三.(每空1分,共11分)
45.(1)镊子(或药匙),稀盐酸;(2)CaCO3+2HCl=CaCl2+CO2↑+H2O;(3)d,c a b d e;
46.(1)
实验一时间较长、温度较高
2KClO3=KCl+3O2↑
实验三将MnO2与KClO3的混合物加热
(2)对比(或比照等);
(3)第一方面:比较MnO2在KClO3分解前后的质量;
第二方面:验证从反应后的剩余物中分离出的物质是否能加快KClO3的分解。
四.(10分)
47.(4分)
解:(1)钾肥中钾元素与硫元素与氧元素的质量比为:39︰16︰32(2分)
(2)K%=钾元素的相对原子质量之和/K2SO4的相对分子质量=2×39/174×100%=44.9% (2分)
48. (6分)
解: (1)由图可知,生成BaSO4沉淀的质量为23.3 g (1分)
(2)设BaCl2的质量为x,生成NaCl的质量为y
BaCl2 + Na2SO4 = BaSO4↓+ 2NaCl
208 233 117
X 23.3 g y
x=20.8 g (1分)
y=11.7 g (1分)
溶液的总质量=29.1 g + 94.2 g + 100 g -23.3 g=200 g (1分)
溶质的总质量=11.7 g + (29.1 g—20.8 g)=20 g (1分)
NaCl%=20/200×100%= 10% (1分)
答:生成沉淀23.3 g,所得NaCl溶液的质量分数为10%。
(注:其他解法,只要合理,结果正确,均可给分。)